|
Grupo funcionalEn química, un grupo funcional es una cadena o conjunto unido a una cadena carbonada, representada en la fórmula general por R para los compuestos alifáticos y como Ar para los compuestos aromáticos y que son responsables de la reactividad y propiedades químicas de los compuestos orgánicos.[1] Se asocian siempre con enlaces covalentes al resto de la molécula. La nomenclatura química de los compuestos orgánicos se basa en la combinación de los prefijos (función secundaria) y sufijos (función principal) asociados a los grupos funcionales junto con los nombres de los alcanos de los que derivan al acceder a los átomos. Series homólogas y grupos funcionales más comunesUna serie homóloga es un conjunto de compuestos que comparten el mismo grupo funcional, por ende poseen propiedades y reacciones similares. Por ejemplo: la serie homóloga de los alcoholes primarios poseen un grupo OH (hidroxilo) en un carbono terminal o primario. Las series homólogas y grupos funcionales listados a continuación son los más comunes.[2] En las tablas, los símbolos R, R', o similares, pueden referirse a una cadena hidrocarbonada, a un átomo de hidrógeno, o incluso a cualquier conjunto de átomos. SaturadosInsaturados
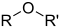
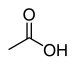
Funciones oxigenadas ruloPresencia de algún enlace carbono-oxígeno: sencillo (C-O) o doble (C=O)
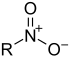
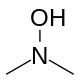
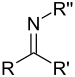
Para consultar la nomenclatura de estos grupos funcionales, consulte Nomenclatura de funciones orgánicas con oxígeno. Funciones nitrogenadasAmidas, aminas, nitrocompuestos, Nitrilos. Presencia de enlaces carbono-nitrógeno: C-N, C=N o C≡N
Funciones halogenadasCompuestos por carbono, hidrógeno y halógenos.
Véase también: Organohalógeno
Grupos que contienen azufre
Véase también: Compuesto de organoazufre
OrganofosfatosVéase también: Compuesto organofosforado
Grupos que contienen metales
[nota 1] El flúor es demasiado electronegativo para unirse al magnesio; se convierte en una sal iónica en su lugar. Nombres de radicales o fraccionesEstos nombres se utilizan para referirse a los propios restos o a especies radicales, y también para formar los nombres de haluros y sustituyentes en moléculas más grandes. Cuando el hidrocarburo original no está saturado, el sufijo ("-il", "-ilideno" o "-ilidino") reemplaza a "-ano" (por ejemplo, "etano" se convierte en "etilo"); de lo contrario, el sufijo reemplaza solo la "-o" final (por ejemplo, "etinoe" se convierte en "etinilo").[5] Cuando se usa para referirse a fracciones, los enlaces simples múltiples difieren de un enlace múltiple simple. Por ejemplo, un puente de metileno (metanodiilo) tiene dos enlaces simples, mientras que un grupo metileno (metilideno) tiene un enlace doble. Los sufijos se pueden combinar, como en metilidino (enlace triple) frente a metililideno (enlace simple y enlace doble) frente a metanotriilo (tres enlaces dobles). Hay algunos nombres retenidos, como metileno para metanodiilo, 1,x-fenileno para fenil-1,x-diilo (donde x es 2, 3 o 4),[6] carbino para metilidino, y tritilo para trifenilmetilo.
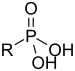
Grupos que contienen fósforoLos compuestos que contienen fósforo exhiben una química única debido a la capacidad del fósforo para formar más enlaces que el nitrógeno, su análogo más ligero en la tabla periódica.
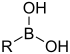
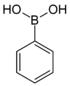
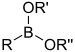
Grupos que contienen boroLos compuestos que contienen boro exhiben una química única debido a que tienen octetos parcialmente llenos y, por lo tanto, actúan como ácido de Lewis.
Véase tambiénNotas
Referencias
Enlaces externos
|







![1,5-Diazabiciclo[4.3.0]non-5-eno (BDN)](http://upload.wikimedia.org/wikipedia/commons/thumb/a/a6/DBN.png/75px-DBN.png)