|
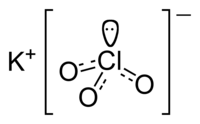
氯酸钾
氯酸鉀由鉀、氯和氧元素組成,化學式為KClO3。它在室溫時是无色晶体或白色粉末,而且是一种强氧化剂,可溶于水和甘油,不溶于醇。其折光率为1.5167[1]。有毒,口服5~10克可致死。[3] 制备
其他制备方法氯酸钾也能通过将氯气通入热的氢氧化钾溶液的方法来制备[5]: 用途氯酸鉀是传統火藥的主要成份,這個成分用到現在都未完全被高氯酸鉀取代。 氯酸鹽系的化學物品因為不易潮解,一直受到火藥製造者的歡迎。然而,氯酸鹽与硫、磷等強還原劑會形成不穩定的爆炸性混合物。因此,氯酸鹽系需於特別設計的設備中使用[來源請求]。氯酸鉀与铝粉的混合物在密閉體系中爆燃可以產生特別的音效,因此被用作爆竹中的爆鸣剂。 作為一種強氧化劑,氯酸鉀可以與許多還原劑形成爆炸性混合物,亦被用於調節某些炸藥的氧平衡,籍以改善其性能。在第一次世界大戰時,曾出現以塑化劑(e.g.:聚异丁烯)和氯酸鉀為主要成分的塑性炸藥,並被用於手榴彈內。不少的火藥都以氯酸鉀取代爆炸性較弱的硝酸鉀。 化学性质氯酸钾与催化剂二氧化锰()进行混合加热到200℃,可以释放出氧气与氯化钾。这种方法是一种常见的实验室製氧法。 其化學反應為: 在酸性溶液中,氯酸盐会被Cl-还原为二氧化氯[6]。氯酸盐也能在酸性条件下和Br-、I-反应,得到相应的单质Br2和I2[7]。 潜在危險 由於氯酸鉀與硫、磷、碳等还原性物质混合後,经摩擦或撞击後就会发生燃烧或爆燃[8],甚至有自發反應的可能性,所以需小心處理,含氯酸鉀的火藥就要避免和硫磺接觸,否則會出現猛烈爆燃[來源請求]。 氯酸钾能使血红蛋白变性并分解,误食会引起急性中毒,致死量为10g[9]。 参考资料
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Index:
pl ar de en es fr it arz nl ja pt ceb sv uk vi war zh ru af ast az bg zh-min-nan bn be ca cs cy da et el eo eu fa gl ko hi hr id he ka la lv lt hu mk ms min no nn ce uz kk ro simple sk sl sr sh fi ta tt th tg azb tr ur zh-yue hy my ace als am an hyw ban bjn map-bms ba be-tarask bcl bpy bar bs br cv nv eml hif fo fy ga gd gu hak ha hsb io ig ilo ia ie os is jv kn ht ku ckb ky mrj lb lij li lmo mai mg ml zh-classical mr xmf mzn cdo mn nap new ne frr oc mhr or as pa pnb ps pms nds crh qu sa sah sco sq scn si sd szl su sw tl shn te bug vec vo wa wuu yi yo diq bat-smg zu lad kbd ang smn ab roa-rup frp arc gn av ay bh bi bo bxr cbk-zam co za dag ary se pdc dv dsb myv ext fur gv gag inh ki glk gan guw xal haw rw kbp pam csb kw km kv koi kg gom ks gcr lo lbe ltg lez nia ln jbo lg mt mi tw mwl mdf mnw nqo fj nah na nds-nl nrm nov om pi pag pap pfl pcd krc kaa ksh rm rue sm sat sc trv stq nso sn cu so srn kab roa-tara tet tpi to chr tum tk tyv udm ug vep fiu-vro vls wo xh zea ty ak bm ch ny ee ff got iu ik kl mad cr pih ami pwn pnt dz rmy rn sg st tn ss ti din chy ts kcg ve








![{\displaystyle {\rm {\ 2KClO_{3}{\xrightarrow[{\Delta }]{MnO_{2}}}3O_{2}\uparrow +2KCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/25826e01809c29fe70b6b028afa70b780d7bf4b6)
