|
Пероксид натрия
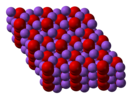
Перокси́д на́трия (пе́рекись на́трия, химическая формула — Na2O2) — бинарное неорганическое химическое соединение натрия с кислородом. При стандартных условиях, пероксид натрия — это желтовато-белые кристаллы с ионной кристаллической решёткой. Является производным пероксида водорода. СвойстваПероксид натрия является сильным окислителем. Энергично взаимодействует с водой со значительным выделением тепла: При определённых соотношениях, а также при использовании подогретой воды происходит опасное вскипание и разбрызгивание подщелоченной воды, поэтому она требует защиту от разбрызгивания и контроль температуры. Особая опасность в том, что при попадании на влажные поверхности, включая кожу, реакция продолжается, а щёлочь и кислород проводят собственные последующие реакции с органикой. Для пероксида натрия свойственно образование хорошо кристаллизующихся гидратов и аддуктов с пероксидом водорода. Так, быстрой кристаллизацией пероксида натрия из ледяной воды легко осаждается гидрат Na2O2·8H2O. С восстановителями, такими, как сера, порошок алюминия, эфиры реагирует с образованием пламени. С монооксидом углерода реагирует менее активно, образуя карбонат: Окисление аммиака пероксидом натрия приводит к образованию нитрата натрия: Действие разбавленными кислотами на пероксид натрия с образованием пероксида водорода: Реагирует с сернистым газом, реакция ускоряется пероксидом водорода и серной кислотой: ПолучениеПрименениеПрименяют для отбеливания тканей, шерсти, шёлка, древесной и вискозной массы, соломы. Для получения кислорода, поглощения угарного и углекислого газа используется в регенерационных установках и изолирующих противогазах: Физиологическое действие и токсикология
Литература
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||